一、课程说明
作为医疗器械制造商,面对法规审核多、合规成本高、市场拓展周期长,使得产品上市和售后监督面临不少挑战。采取什么样的方案和提交什么样的报告可被视为符合多国QMS要求和法规的证据?医疗器械单一审核方案(MDSAP)是国际医疗器械监管机构论坛(IMDRF)成员共同发的项目,能够帮助您的企业一站式满足不同国家监管机构要求,实现一次进入多元市场。
• MDSAP审核架构和范围
• MDSAP审核和QMS审核的区别
• MDSAP文档的识别
• MDSAP五国的不同的法规简介
• MDSAP审核的七大过程要求
二、适用对象
有ISO 13485和质量管理体系的基础,希望了解更多有关MDSAP的信息
负责企业的质量管理体系和MDSAP项目
医疗器械企业的QA/RA
企业生产的产品上市国涉及MDSAP参与国(美国、加拿大、巴西、日本、澳大利亚)
三、课程收益
提升法规监管的审核技巧
五国法规对比解析,节省法规调研时间,降低注册驳回风险
全流程+审核报告解析,提升内部团队专业性,缩短周期
有效应对您指定审核机构的MDSAP审核
四、讲师介绍
就职于知名国际认证机构,ISO13485主任审核员、欧盟CE认证评审专家、医疗器械行业资深主任培训讲师;
三十年以上的医疗器械行业质量管理工作经验,二十年以上的医疗器械质量体系审核、CE产品评审工作经验,十五年以上的医疗器械培训经历;
熟悉各国医疗器械注册和体系法规,熟悉医疗器械的设计生产各活动的质量管理,审核和培训过上千家国际知名企业,善于结合企业最佳实践案例深度讲解国际法规与实施问题。
五、培训日程
时间 | 主要内容 |
13:30-16:30 | 一 MDSAP基础知识 二 MDSAP审核架构和范围 - MDSAP的审核流程及其相互关系 - MDSAP和企业合规 - MDSAP审核报告和审核发现分类 三 MDSAP审核和其他QMS审核的区别 四 MDSAP文档的识别 五 MDSAP五国不同法规简介,包含上市前和上市后的法规,以及变更报告的要求 - 美国QSR 820,803、806、807、821 - 加拿大CMDR - 巴西GMP、Pre-Market Approval、PMS - 日本法规No.169 - 澳大利亚TGA MDR 六 策划审核范围 |
16:30-17:00 | 交流答疑 |
时间 | 第二天 主要内容 |
9:00-16:30 | 一 MDSAP审核的七大流程要求 - 管理流程 - 测量、分析及改进流程 - 设计和开发流程 - 生产和服务控制流程 - 采购流程 - 产品市场授权和注册流程 - 医疗器械不良事件和忠告性通知流程 二 如何审核医疗行业和不同的法规要求 三 使用正确的监管术语 |
16:30-17:00 | 交流答疑 |
六、培训费用
1、非联盟1980元/人
2、19800 元联盟单位:制药+医械课程全部免费听课
3、11800 元医械联盟单位:免费听课
4、6000元医械联盟单位:700元/人
5、3000 元医械联盟单位:980 元/人
七、汇款信息
公司名称:石家庄允咨医药科技有限公司
开 户 行:招商银行股份有限公司石家庄广安支行
账 号:311901602310701
*公对公汇款请注明:6月五国联审课程
*个人垫付汇款请注明:公司名称+6月五国联审课程
八、培训证书
培训结束由允咨培训中心颁发培训证书,此证书包含12学时培训证明,可作为医疗器械专业技术人员聘用、晋升、职称评定、继续教育或申报评定资格重要依据和职业能力考核的重要证明。


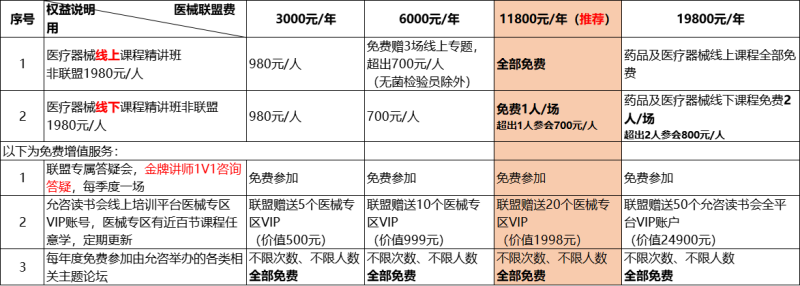
允咨医械培训联盟:为降低企业培训成本,加入允咨医械培训联盟,具体权益如下: