【8月21日 线上】有源医疗器械注册申报实战专题培训
发布时间: 2025-07-31 14:50
时 间: 2025年8月21日
地 点: 线上
一、课程背景
在医疗器械监管持续趋严的背景下,有源器械注册因涉及电气安全、软件验证、复杂临床评价等环节,成为企业产品上市的“高发雷区”。本次课程聚焦有源医疗器械,直面企业注册痛点,以“零退回、高效率、强合规”为目标,攻克注册材料核心难点帮助有源器械企业注册人员建立合规高效的注册体系,缩短上市周期,降低发补率,节约人力与时间成本。欢迎企业相关人员积极参加。
二、适用对象
有源医疗器械企业的研发人员、注册人员、临床人员等专业人士
三、讲师介绍
李老师
高级工程师/执业药师、西班牙武康大学博士学位,中南大学硕士学位;吉林省药监局兼职注册检查员;湖南省生物材料学会专家及长沙市青年科技工作者协会理事;第二届湖南省医疗器械行业协会副会长。
▶ 15年实战纵深覆盖
专注医疗器械注册策略、临床评价、质量管理体系及洁净厂房设计,主导完成:
✓ 50+项二类/三类医疗器械产品注册(含20余项III类有源器械)
✓ 30+个临床试验项目管理(含多中心RCT)
✓ 20万级/10万级洁净厂房合规性设计项目12项
四、培训时间安排及内容
8月21日 9:00-17:00 |
时 间/讲 师 | 课程内容 |
9:00-16:30 李老师 | 1有源医疗器械产品注册 1.1有源医疗器械产品注册通用要求 有源器械注册法规体系与核心要求 申报全流程详解 质量管理体系与注册的协同 (DHF与DMR的关联性、注册体系核查的核心关注点及应对准备、如何确保注册资料与体系文件的一致性) 1.2有源医疗器械注册申报资料全景图与核心资料撰写实战 综述资料、研究资料、 风险管理、产品性能研究 生物相容性评价、 稳定性/有效期研究: 临床评价资料 常见退审/发补点深度剖析 1.3有源医疗器械注册共性问题与规避策略 例:技术要求制定不合理 研究资料不充分 临床评价路径选择错误或论证不充分 产品变更管理 审评发补问题的高效应对技巧与沟通策略 1.4有源医疗器械注册申报路径的选择 2案例分享:手术动力设备产品注册 2.1手术动力设备医疗器械产品注册技术审查指导原则 2.2电动骨组织手术设备产品技术要求 2.3骨科动力手术设备临床评价路径选择及准备 |
16:30-17:00 | 交流答疑 |
五、培训费用
1、非联盟1400元/人
2、19800 元联盟单位:制药+医械课程全部免费听课
3、11800 元医械联盟单位:免费听课
4、6000元医械联盟单位:500元/人
5、3000 元医械联盟单位:700 元/人
六、汇款信息
公司名称:石家庄允咨医药科技有限公司
开 户 行:招商银行股份有限公司石家庄广安支行
账 号:311901602310701
*公对公汇款请注明:8月有源注册课程
*个人垫付汇款请注明:公司名称+8月有源注册课程
七、培训证书
培训结束由允咨培训中心颁发培训证书,此证书包含8学时培训证明,可作为医疗器械专业技术人员聘用、晋升、职称评定、继续教育或申报评定资格重要依据和职业能力考核的重要证明。


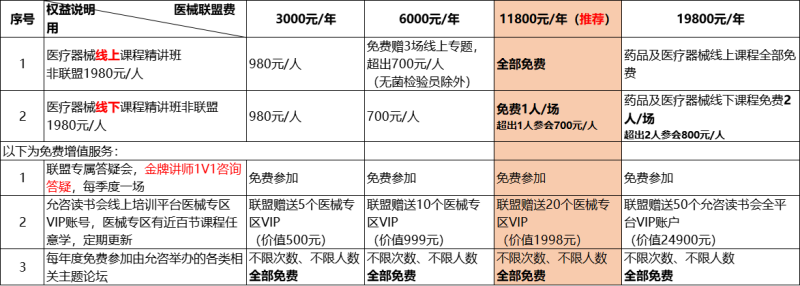
允咨医械培训联盟:为降低企业培训成本,加入允咨医械培训联盟,具体权益如下: